현재 여러 전기자동차에서 사용되고 있는 에너지원인 리튬이온 전지에 대해서 적어보도록 하겠습니다.

리튬 이온 셀은 보통 원통형, 선형, 파우치 이렇게 3가지의 형태로 시장에서 쓰이게 됩니다.

활성 전극의 재료는 금속 포일과 같은 재료로 코팅되어 있습니다. 금속 포일은 셀에 유입, 유출되는 전류에 대한 전류 집전 역할을 수행합니다.
셀 형태에 따라서 기본적인 2가지 전극 구조가 있습니다.
* Pouch cell과 같은 Stacked 구조
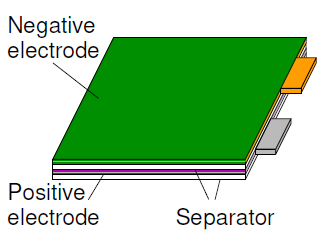
해당 구조는 작은 주머니(Pouch) 같은 형태로써 높은 용량을 지닌 배터리에서 공간의 최적화를 위해서 사용되어지는 구조입니다. Pouch 구조는 stacked 전극 구조로써 음극과 양극 포일이 각각의 전극 판으로 나눠져서 stack 되어 있으며 둘은 분리막(Separator)을 통해서 나눠져 있습니다. 분리막(Separator)은 동일한 전극과 같이 동일한 사이즈로 잘릴 수 있으며 그러나 종종 분리막이 더 긴 형태를 지니기도 합니다.
모든 음극 양극 탭은 평행적으로 용접되어 있으며 셀의 음극, 양극 접점(terminal)과도 붙어있습니다.
* 원형 또는 선형의 셀 형태로 Spiral Wound 구조

원형의 구조는 음극과 양극 포일이 2개의 긴 조각으로 와인딩의 축이 되는 Mandrel에 감겨있습니다. 또한 분리막과 같이 위치하며 전극이 분리되는 것을 잡아주는 역할을 합니다.
대부분의 선형 Cell 같은 경우 원통형 구조와 비슷하게 제조되며 다만 평평한 Mandrel에 감겨있습니다.
리튬 이온 전지 장 단점
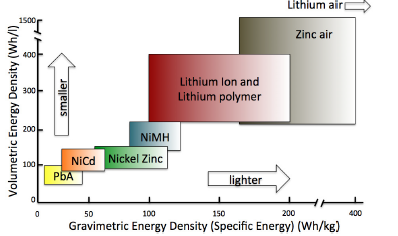
타 배터리 같은경우(Ni,MH, NiCd) 1.2V의 전압을 가지지만 리튬 이온 배터리는 무려 3.7V의 전압을 가지기 때문에 고출력, 고전압을 기반으로 하는 전기자동차 내부에서 많이 사용되게 됩니다.
보통 NiMH이나 NiCd 같은 경우 다른 전자기기에 연결이 되어 있지 않아도 하루에 자가방전을 통한 1~5%의 Drop이 일어나지만 다른 2차 전지보다 낮은 자가방전율 특성을 가지기 때문에 오랜시간 동안 방치되어도 리튬이온 전지 같은 경우 충전 상태를 오랜시간 유지가 가능합니다. 수명 또한 더 부드러운 Intercalation 현상을 가지기에 더 긴 수명을 가질 수 있습니다.
그러나 단점으로는 리튬 이온 배터리 같은 경우 동일한 Capacity를 가질 때 NiMH나 NiCd보다 상대적으로 가격이 비쌉니다. 또한 제조하기가 어렵기 때문에 NiMH 또는 NiCd 배터리보다 생산량이 적음 높은 에너지의 밀도는 더 활성화된 화학반응에서 오기 때문에 덜 안전하며 특별한 안전 수칙이 따로 필요함. 또한 과충전 방전에 따른 배터리를 보호하기 위한 특별한 회 로또 한 필요로 함. 추가적으로 불순한 Cell 성분이나 제작사마다 비슷한 화학 구성물을 사용하지만 다른 성능을 보일 수도 있기에 시스템에 영향을 줄 수도 있습니다.
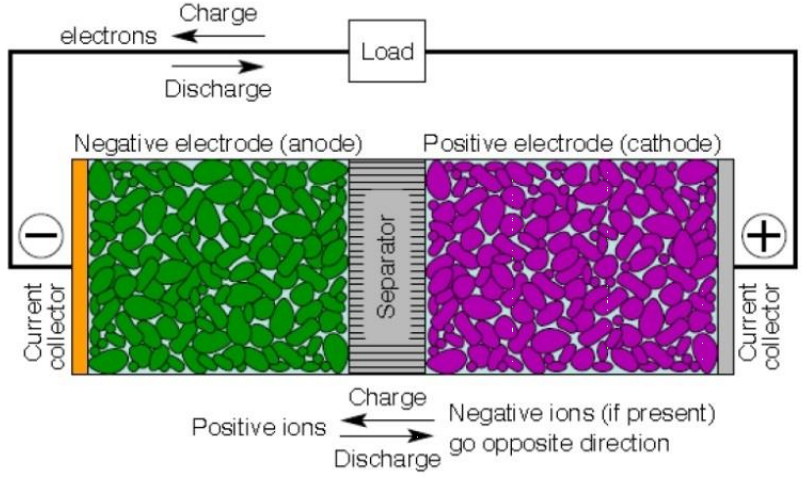
- 충, 방전 과정 ( Charge & Discharge Process in LIBs )
방전 과정 동안에는 리튬이 음극의 표면을 떠나면서 전자를 주게 됩니다. 결국 Li은 양이온이 되어 전해질로 들어가게 됩니다. 리튬은 음극의 중심부에서 바깥쪽으로 diffuse 되는데 농도의 균형을 맞추기 위해서 Li이 한동안 양극으로 흘러들어 가게 됩니다.

반면 전자는 외부 회로를 통해서 양극으로 이동하게 됩니다. 리튬 양이온은 전자와 만나게 되며 리튬은 양극의 표면으로 들어가게 됩니다.

충전 과정 동안 Li은 양극의 표면에서 빠져나가서 전자를 주고 다시 리튬 양이온 상태로 전해질로 들어가게 됩니다.
반면 전자는 Charger에 의해서 강제적으로 외부 회로로 가서 음극으로 이동하게 됩니다. 그때 Li 양이온과 전자가 만나고 그리고 리튬은 음극의 표면으로 다시 들어가게 됩니다. 리튬의 확산은 마찬가지로 양쪽 극에서 내부의 농도를 맞추기 위해 진행됩니다.
그리고 리튬 이온전지는 다른 배터리와 다르게 Intercalation 과정을 거치게 됩니다.
intercalation은 층상구조가 있는 물질의 층간에 분자· 원자와 이온이 삽입되는 현상을 말합니다. 이렇게 이온들이 결정 내로 들어가면, 결정의 전자 구조도 바뀌게 되어, 외부 도선을 따라 전자가 들어가게 됩니다. 마치 리튬이 전극에 보관되어있는데 마치 스펀지가 흡수한 물처럼 보관되어 있는것처럼 생각하면 되겠습니다.
방전 때 음극에 intercalation 되어있던 리튬이 환원 전위 차이로 산화반응을 통해 양극으로, 전자는 도선을 통해 이동하고 양극에서 환원 및 intercalation되며 충전 상황에서는 외부적인 힘으로 양극에서 방출된 리튬이온이 음극에 있는 흑연 내부로 intercaltion됩니다.

- 전극 (Electrode)
전극은 단일의 물질로 구성되어있는 블록이 아닌 백만 개의 작은 입자로 구성되어 있습니다. 하단의 사진은 전극의 단면을 보여주는 사진이며 해당 구조를 통해서 접촉면적 또한 늘어나며 cell의 저항이 감소되며 파워의 Capability 또한 상승하는 장점을 가지게 됩니다.

주된 전극 재료로는 재료들을 묶어주는 Binders와 전자의 전도성을 높여주는 Conductive additives로 구성됩니다.
- (전극) 음극 및 양극의 재료 및 구조
음극은 주로 graphite(흑연)으로 구성되어 있습니다. 흑연은 오늘날 아주 필수적으로 모든 리튬전지의 음극에 사용되며 구조적으로 안정성과 낮은 전자 화학 반응성, 많은 리튬 이온 저장 능력, 저렴한 가격 등의 조건을 갖추고 있기 때문입니다.
흑연은 보통 그래핀 층으로 구성되는데 매우 강력하게 결합된 구조로 되어 있습니다. 이러한 층은 대신 느슨하게 stack 되어 있으며 층과 층의 공간 사이에는 리튬이 intercalate 즉 층간 결합을 수행하는 곳이 되겠습니다.

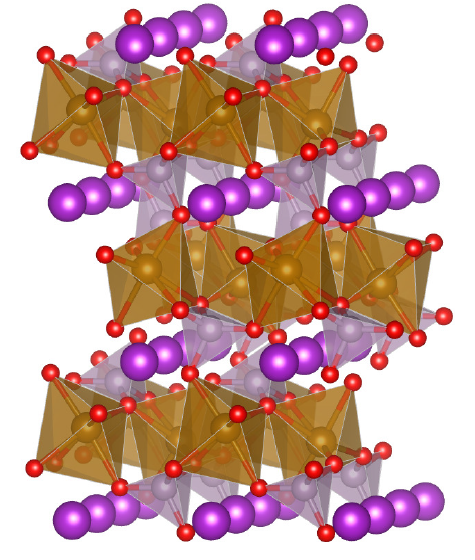
대안으로 사용되는 음극의 재료로는 LTO가 있습니다. LTO는 Lithium titanate oxide( 리튬 티탄산화물 ) 이 사용됩니다. 해당 재료는 흑연과 다르게 매우 다른 구조를 가지는데 사진에서 리튬 : 보라색, 티탄 : 주황색, 산소 : 빨간색으로 초록색 다면체의 결정 구조를 가집니다.
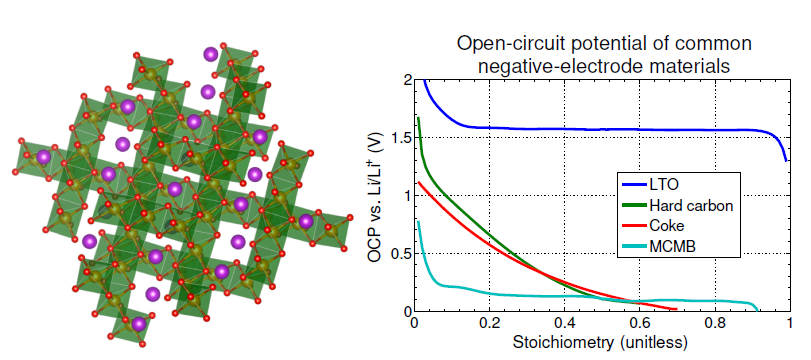
LTO의 단점은 다만 높은 Open-circuit Potential을 가지는데 때문에 셀의 전압이 낮아지게 됩니다. 장점으로는 거의 파괴되지 않기에 매우 긴 수명을 가집니다.
또 하나의 대체제로써 미래의 음극 구조로써 떠오르는 재료는 실리콘입니다.
실리콘은 매우 유망한 음극 재료로써 보통 흑연을 사용하였을 때 6개의 탄소 원자에 Li을 보관할수있었다면 실리콘을 사용하였을때는 실리콘 한개의 원자당 4개를 저장할수있기 때문에 더 높은 에너지 밀도를 기대할수있습니다. 다만 흑연으로 사용하였을때 충 방전 과정에서의 부피 변화가 10%인 반면 실리콘 같은 경우 무려 400%의 변화를 가집니다. 때문에 실리콘 전극은 매우 쉽게 부서지며 짧은 수명을 가지게 됩니다.
때문에 다른 대안으로는 흑연과 실리콘을 혼합하여 제조하거나 또는 작은 nanowire 숲을 실리콘으로 만들어서 팽창에 대해서 대비하게끔 만드는 방법이 있습니다.
양극의 재료로써 많은 후보 재료들이 존재합니다. 1980년에 John B.Goodenough는 LCO(Lithium cobalt oxide)로 리튬의 intercalation이 가능한 물질이라는 것을 발견하였습니다. 리튬은 CoO6 octahedra 층에 intercalates 되며 LCO 또한 층이 존재하는데 흑연과 비슷하며 또는 종종 “layered cathode”라고 불립니다.

LCO는 보편적으로 크기를 확대하면 문제가 생김으로써 작은 셀 형태로 사용되는데 보통 휴대 전자기기의 셀에 들어가게 됩니다. 또한 LCO의 구성 성분인 cobalt는 매우 드물며 독성이 있고 매우 값이 비싸기도 한 이유도 있습니다.
Ni은 Co로 대체가 가능하며 Co는 더 높은 에너지 밀도(동일한 Capacity에서 더 높은 전압)를 제공해줄 수 있습니다. 그러나 Co 같은 경우 매우 열적으로 안정적이지 않은 단점이 있습니다. 마찬가지로 Al(알루미늄), Cr(크로뮴) , Mn(망간) 또한 대체 재료가 될 수 있는데 당연히 다른 재료들을 쓰기 때문에 재료의 특성들을 고려해서 제작되어야 합니다.
1983년 Goodenough와 Thackery는 Li(x) Mn(2) O(4) 즉 LMO 가 intercalation 재료로써 다른 대체제가 될 거라고 제안하였습니다. Mn은 팔면체 위치에 있으며 Li은 사면체 구조에 위치해 있습니다. 이 재료는 입방체의 spinel 구조로 이루어져 있으며 3차원 적인 확산이 가능합니다.

Li(x) Mn(2) O(4)에서 x는 0에서 1 사이의 값을 가지게 됩니다. 그러나 2 이상으로 가질 수도 있는데 그때 LMO가 산성 조건이 불안한 상태가 됩니다.
LMO의 장점은 가격이 저렴하며 또한 LCO보다 매우 안전합니다. 그러나 몇몇 특정한 조건에서 망간이 전해질로 용해를 하기 때문에 짧은 수명을 가지게 됩니다. 이러한 문제점을 해결하기 위해서 Additives(첨가제)가 더해지는데 이러한 기술은 매우 비밀스럽게 산업에서 적용되어 있다고 합니다.
1997년에는 Goodenough는 olivine 형태의 인산염을 3번째 주요 양극 재료의 항목으로 제안하였습니다. LFP ( Li(x) FePO(4) )는 이러한 범주 안에서 보편적으로 사용되는 재료이며 해당 재료는 저렴한 가격과 낮은 독성을 가지는 이점이 있으나 다만 low open-circuit potential에 의한 낮은 에너지 밀도를 가지며 Fe의 무거움으로 인하여 낮은 에너지를 가지는 특성을 지닙니다.
1차원 구조는 보통 높은 저항을 가지는 성질을 보이는데 매우 작은 입자들과 전도성 첨가제를 사용하여 이러한 성질을 극복할 수 있습니다.
* 양극의 재료로써 더 많은 후보들이 존재하는데 대부분 위에서 언급한 재료들의 혼합으로 이뤄집니다.

- 전해질 ( Electrolytes for lithium-ion cells )
전해질의 재료로는 보통 소금, 산 그리고 이온들이 전극 사이를 이동하게끔 하는 매체 역할을 수행하는 재료로 구성됩니다. 매체 역할을 해야 하기 때문에 전해질은 보통 순수하게 이온의 거동에 대한 conductor 역할을 수행하는데 화학적 반응에는 기여하지 않습니다.
셀에서 수성(Aqueous, 물에 녹는) 전해질을 사용했을 때는 2V 이하의 한계를 가집니다. 물은 더 높은 전압에서 산소와 수소로 분해되기 때문입니다. 때문에 전체적인 전압이 2V를 초과할 때 리튬 이온 셀은 전해질로써 수성이 아닌 organic의 용매제를 첨가하여 만듭니다
용매는 ethylene carbonate, propylene carbonate, dimethyl carbonate, ethyl methyl carbonate, diethyl carbonate 이렇게 5개를 포함합니다.
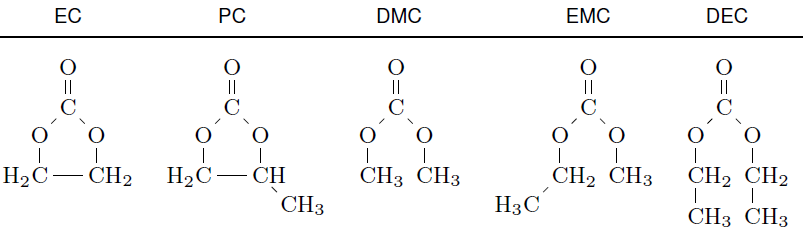
공통의 특징으로써 이러한 용매제는 약간의 음극을 가지는 산소의 이중결합을 포함하며 분자를 분극 화하여 소금을 녹이도록 합니다. 소금은 매우 보편적으로 LiPF(6) - Lithium hexafluorophosphate 셀에 사용됩니다. 소금은 다른 화학적 반응에 반응하지 않는 특성을 지녔기에 보편적으로 전해질 재료에 사용됩니다. 또한 소금은 LiBF(4) - LiBF4 (lithium tetrafluoroborate) and LiClO(4) (lithium perchlorate)에도 들어가 있습니다. 때문에 종종 전해질이 다른 용매제를 포함하더라도 그냥 소금물이라고 불리기도 합니다.
- 분리막 (Separator)
분리막에 필요한 특성은 극간의 전기적 단락 방지를 위한 절연성, 전기화학적 안정성, 기계적 강도, 막 두께, 셧다운 등이 이 존재합니다. 막 두께는 전지의 고용량화에 필요하고, 셧다운은 안정성에 중요합니다.
하단의 분리막 사진을 보면 작은 구멍들이 보입니다. 분리막은 투과가 가능한 막으로 Li 양이온을 충분하게 방해 없이 통과시킬 수 있는 구멍이 포함되어 있습니다. 그러나 음극 및 양극의 입자들은 충분하게 통과하지 못하게 하는 구멍을 가지고 있기에 short-circuit 현상을 막는 역할도 수행하고 있기에 Electronic insulator 역할로 존재합니다.

사진에서 분리막은 매우 얇은 백색의 플라스틱 같이 생겼으나 확대를 하면 매우 많은 구멍(pores)들이 존재하는 것을 확인할 수 있습니다. 맨 오른쪽 그림은 LMO와 상대적인 크기를 보여주는 사진으로 전극의 입자는 절대로 통과 못하는 구멍 크기로 구성된 것을 보여주고 있습니다.

사용되는 목적에 따라 10~30㎛ 정도의 두께를 가지며, 상호 연결된 구조의 0.1~1㎛의 기공크기를 갖는 폴리에틸렌 또는 포리프로필렌 같은 폴리올레핀계 고분자 재료로 구성됩니다.
- Current Collectors
배터리를 구성하는 마지막 재료는 Current Collectors 즉 전류 집전장치입니다. 리튬 이온 셀 안에는 매우 가혹한 환경으로 되어 있는데 Li과 F는 특히 매우 reactive 한 원소입니다. 전류 집 전기는 때문에 이러한 환경을 견딜 수 있어야 하며 전해질과는 반응을 하지 않아야 하는 조건을 만족해야 비로소 집전장치로써의 조건을 만족했다고 할 수 있습니다. 그러면서 전기 저항이 낮으며, 충방전 중에 활물질로/에서 전류 전달하도록 구성되어야 하는데 양극에 사용되는 집전장치의 재료는 알루미늄 포일이 사용되며 알루미늄 포일은 매우 높은 potential 영역을 지니고 있습니다. 또한 전해질과 반응하지 않는 성질을 가지고 있기 때문입니다.
음극에서는 구리 포일이 사용되며 마찬가지로 전해질과 반응되지 않습니다.
* 정리
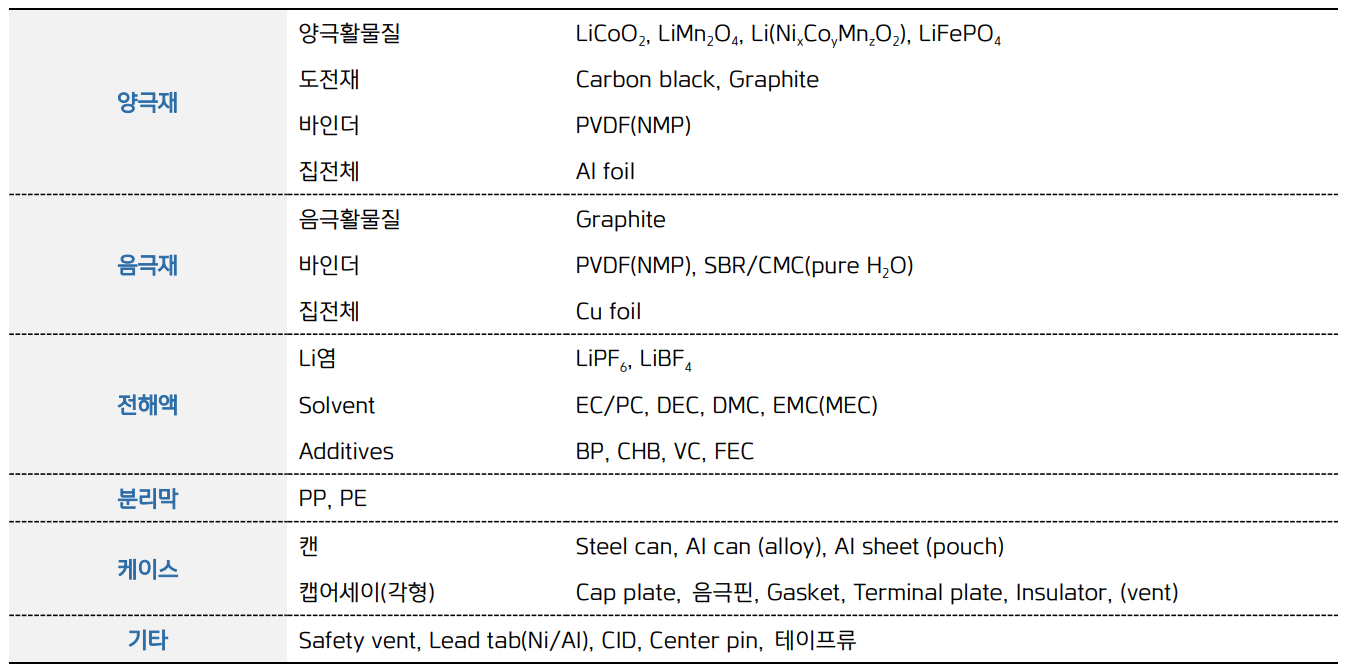
마지막으로는 리튬이 현재 고갈되고 있는가 라는 의문에 대한 것입니다.
현재 수많은 전기자동차가 생산되고 있으며 후에 지금의 내연기관 자동차 시장의 파이를 동일하게 전기자동차로 대체하면서 더 확장될 예정입니다. 각각의 전기자동차에는 일정 양의 리튬이 들어가야 하는데 밑의 사진은 현재 리튬의 매장량에 대한 조사를 한 것입니다.

해당 사진에서 Li은 왼쪽 중상의 위치에서 존재하는데 Pb나 Ni보다 20~100배 정도 더 풍부하게 매장된 것으로 조사되었습니다. Li은 매우 reactive 하여 자연에서 찾기가 힘든데 때문에 Compound 한 물질에서 추출하게 됩니다.
리튬이온 셀에서는 꽤나 적은 리튬을 함유하고 있습니다. LCO 셀( 양극이 LiCoO2로 구성된 셀)을 볼 때 LCO는 전체 무게의 33% 이하로 차지하고 있으며 LCO에서 리튬은 7%를 차지하게 됨으로써 리튬은 전체 셀 무게에서 2%의 비중으로 구성하고 있습니다. 전해질 또한 일정한 리튬을 가지고 있는데 전체 셀의 10%의 무게를 차지하고 있기에 결론적으로 리튬은 전체 셀의 3% 이하를 차지하고 있습니다. 200 마일의 전기자동차는 60 Kwh의 배터리가 필요로 한데 리튬은 각 차량당 12kg만큼 들어가 있습니다. 백만의 전기자동차는 재활용 없이 12000톤의 리튬을 소비하게 되는데 마찬가지로 백만 개의 PHEV 또는 HEV 차량은 1200톤 이하로 소비하게 됩니다.
이러한 결과는 곧 이 말은 즉 전 세계의 인구가 각자 1000대 이상의 전기자동차를 가져도 충분하다는 결과인데 매우 믿을 수 있는 정보 조사 매체에서 나온 거라고 합니다.
최근 2020 12/4 "포스코, 남미 소금호수 '대박'... 리튬 매장량 전기차 약 3억 7천만 대 생산가능" 라는 기사가 나왔습니다. 현재 포스코가 보유하고 있는 아르헨티나 ‘옴브레 무에르토’ 소금호수는 최종 매장량 평가 결과 인수 당시 추산한 220만 톤 보다 6배 늘어난 1350만 톤인 것으로 확인되었는데 이는 곧 이는 전기차 약 3억 7천만 대를 생산할 수 있는 수준으로 다른 지역의 리튬 양과 재활용되는 전지를 생각한다면 당분간은 리튬을 이용한 전지가 꾸준히 사용될 예정이라고 판단되어집니다.

Reference
- Introduction to battery-management systems ( 1.2.1~1.2.7 )
- 키움증권 리서치 센터 "차세대 배터리 미래를 담을 기술"
'전공 관련 (Major) > 강의 (Lecture)' 카테고리의 다른 글
| 6. Battery Management System 구성 및 기능들 (2) | 2021.01.15 |
|---|---|
| 5. Battery Management System의 5가지 조건 (2) | 2021.01.14 |
| 2.전기화학 전지 구성 및 과정 (0) | 2021.01.10 |
| 1. 배터리 관련 개념 및 용어 정리 (0) | 2021.01.10 |
| 3. 전기화학 관련 용어 정리 (0) | 2021.01.10 |




댓글